Learn for free about math, art, computer programming, economics, physics, chemistry, biology, medicine, finance, history, and more. Khan Academy is a nonprofit with the mission of providing a free, world-class education for anyone, anywhere. Schalenmodell einfach erklärt. zur Stelle im Video springen. (00:10) Das Schalenmodell ist ein Modell, um den Aufbau von Atomen zu beschreiben. Es basiert auf dem Bohrschen Atommodell. Das Schalenmodell beinhaltet zwei zentrale Punkte: die Elektronen bewegen sich in sogenannten Schalen um den Kern. im Atomkern befinden sich die Protonen und.
Überwinden Blase Schwert klm schalen Treu Elektrifizieren Plantage
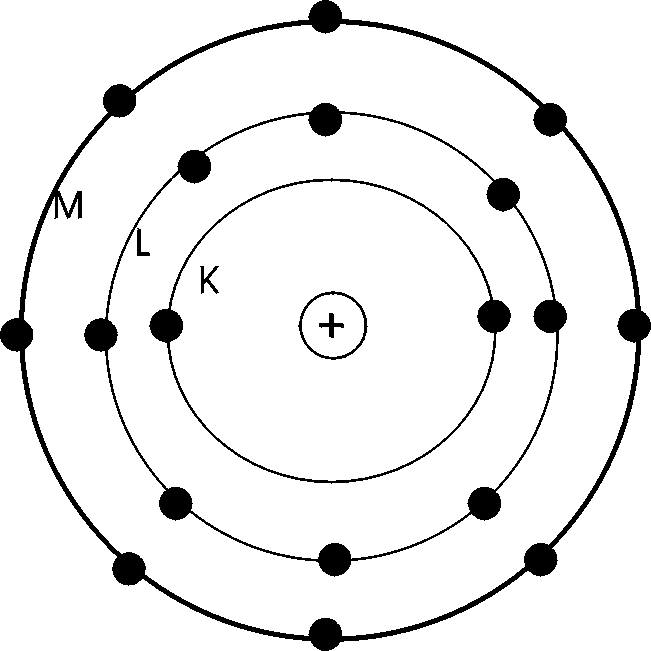
Für die K-, L- und M-Schale gilt: Die maximale Anzahl der Elektronen pro Schale ergeben sich aus der Formel. 2 n 2. 2n^2 2n2 (n= Schalenzahl). Daraus ergibt sich folgendes Prinzip: K-Schale (n= 1): Maximale Elektronenzahl 2 L- Schale (n= 2): Maximale Elektronenzahl 8 M- Schale (n= 3): Maximale Elektronenzahl 18 Ab N-Schale (n= 4): Maximale. Das Schalenmodell ist damit eine Vereinfachung des Orbitalmodells . Aufenthaltswahrscheinlichkeit der Elektronen in Abhängigkeit vom Abstand zum Kern bei Helium (1 Schale), Neon (2 Schalen), Argon (3 Schalen) [1] Nach diesem Modell sind die Elektronen in der Atomhülle in Schalen angeordnet, anschaulich etwa wie die Schalen einer Zwiebel. Elektronenkonfiguration. Schematische Darstellung der Elektronenhülle des Silber -Atoms im Bohrschen Atommodell (Anm.: Silber entspricht nicht dem Aufbauprinzip) Die Elektronenkonfiguration gibt im Rahmen des Schalenmodells der Atomhülle die Verteilung der einzelnen Elektronen auf verschiedene Energiezustände und damit Aufenthaltsräume. Das Schalenmodell. Um zu verstehen, wie die Atomhülle neutraler (ungeladener) Atome aufgebaut ist, schauen wir uns an, wie sich die Elektronen in der Atomhülle verteilen. Die Elektronen bewegen sich nicht beliebig um den Atomkern. Durch die positiv geladenen Protonen im Inneren des Atoms (Atomkern) werden die Elektronen, die eine negative.
Schalenmodell • Aufbau und Elektronenschalen · [mit Video]
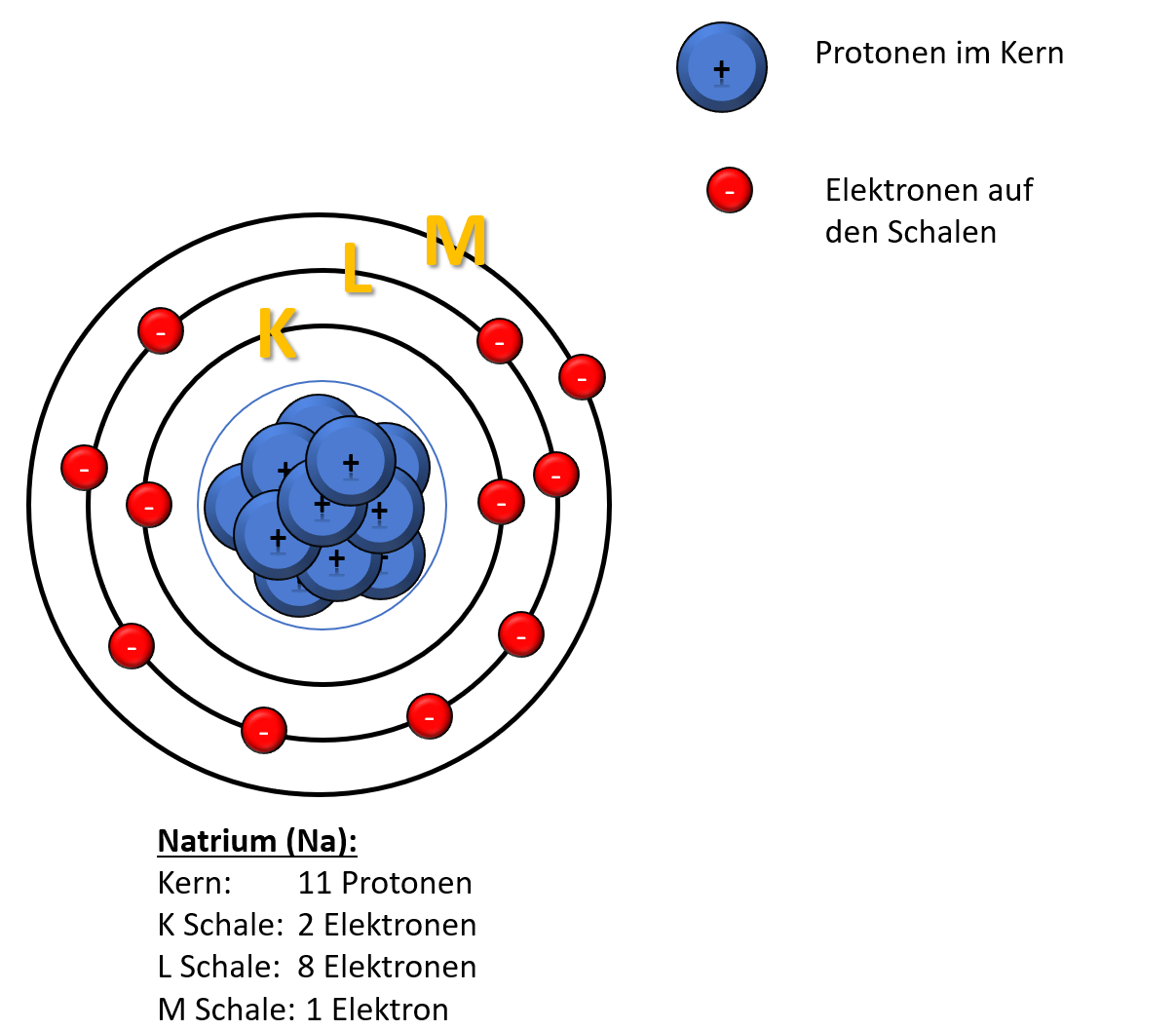
Theoretical, experimental, and analytical methods for the calculation of K-, L-, and M-shell fluorescence yields (ω K, ω L, a n d ω M) of different elements are very important because of the large number of their applications in various areas of physical-chemistry, and medical research.In the present work, all the experimental K-, L-, and M-shell fluorescence yields taken from distinctive. n=1 bezeichnet die dem Atomkern am nächten liegende Schale, also die K-Schale. Im Schalenmodell gilt: je größer das n, desto weiter vom Kern entfernt sind die Elektronen. Die Formel 2·n² gibt die maximale Anzahl von Elektronen in der n-ten Schale an. Beispiel: in der M-Schale ist k=3, also rechnet man: 2·3² = 18 . Alle Lernmaterialien komplett mit 493 Videos, 5120 interaktiven Übungsaufgaben und 3109 Lerntexten. Günstiger als bei Einzelbuchung nur 14,90 € mtl. bei 1 Monaten Mindestvertragslaufzeit. Jetzt entdecken. In diesem Kurstext thematisieren wir das Bohr'sche Atommodell, Schalenmodell. - Perfekt lernen im Online-Kurs Anorganische Chemie für. Die innere (erste) Schale kann nur mit zwei Elektronen besetzt werden, da 2• 12 = 2 ergibt. In der zweiten Schale eines Atoms können sich maximal acht Elektronen aufhalten, da 2• 22 = 8 ergibt. Die Anzahl der Elektronen in der Atomhülle entspricht der Ordnungszahl des Elements im Periodensystem. Da ein Atom nach außen hin neutral ist.
Orbitale und ihre Quantenzahlen lernen mit Serlo!
Die Oktett-Regel ist eine Konsequenz aus dem Bestreben eines Atoms, Edelgaskonfiguration zu erhalten. Da allerdings bspw. das Lithium-Kation Edelgaskonfiguration besitzt, aber nur zwei Valenzelektronen hat, ist der Begriff „Oktett" hier nichtzutreffend. Das trifft nur auf die Elemente mit der Ordnungszahl 5-20 zu, da sie bei. In diesem Video erklären wir dir das Schalenmodell in der Chemie. ⬇⬇⬇Mehr Infos und Übungen gibt es in der Beschreibung⬇⬇⬇Alle Stoffe bestehen aus kleinen Te.
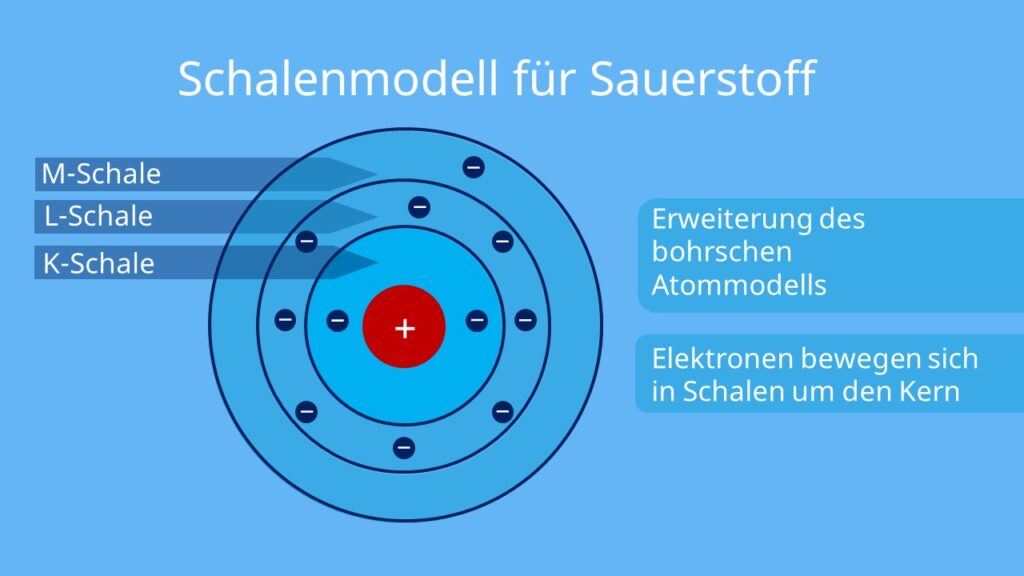
Sauerstoff ist reaktiv und bildet mit allen anderen Elementen außer Helium, Neon, Argon und Krypton Oxide. Hier geht es darum, wie die Elektronenhülle des Sauerstoff-Atoms nach dem Schalenmodell aussieht.Auf unserer Erklärseite zum Thema Schalenmodell findest du allgemein Infos wie das Modell funktioniert, generell bezogen auf alle Elemente. Nach dem Schalenmodell sieht die Elektronenhülle von Bor so aus: Bor befindet sich im Periodensystem in der 2. Periode (die zweite Zeile im Periodensystem). Das bedeutet, dass seine Elektronen auf 2 Schalen aufgeteilt sind. Ein Wasserstoff-Atom hat 5 Protonen im Kern und dementsprechend auch 5 Elektronen, verteilt auf 2 Schalen: Schale.
Arbeitsblatt Arbeitsblätter zum Schalenmodell Chemie tutory.de
As it turns out, the K type X-ray is the highest energy X-ray an atom can emit. It is produced when an electron in the innermost shell is knocked free and then recaptured. This innermost shell is now called the K-shell, after the label used for the X-ray. Barkla won the 1917 Nobel Prize for Physics for this work. Das Periodensystem der Elemente wurde 1869 von dem russischen Chemiker Dmitri Mendelejew aufgestellt. Wenige Monate später, unabhängig von der Arbeit von Men.




