Oefenvragen en meer uitleg? Ga naar https://meneerwietsma.nl/Inhoud video:- Uitleg over verschil tussen zuivere stoffen en mengsels- OefenopgaveHet Natuurk. Mengsels en zuivere stoffen Bijles Scheikunde HAVO Hoe kun je zuivere stoffen herkennen? We gaan eerst eens kijken naar zuivere stoffen. Zuivere stoffen zijn stoffen die je kunt herkennen aan vaste stofeigenschappen. Een zuivere stof kun je het beste herkennen aan hoe de stof kookt of smelt.

PPT 7. Scheiden van zuivere stoffen en mengsels PowerPoint Presentation ID469841
Een mengsel is in de scheikunde een combinatie van twee of meer verschillende zuivere stoffen zonder dat hun moleculen daarbij hun chemische identiteit verliezen. Een mengsel wordt gekarakteriseerd door de moleculen die eraan deelnemen en de verhouding van hun hoeveelheden. 1.3K views 2 years ago. IN DEZE VIDEO In deze video leg ik het volgende uit: het verschil tussen zuivere stoffen, mengsels, verbindingen en elementen, de verschillende soorten mengsels en hun. Mengsel of zuiver stof? Pixabay. Dit is een oefening op het indelen van stoffen in zuivere stoffen of mengsels. Er wordt nog geen onderscheid gemaakt in heterogene of homogene mengsels, noch in enkelvoudige of samengestelde zuivere stoffen. About Press Copyright Contact us Creators Advertise Developers Terms Privacy Policy & Safety How YouTube works Test new features NFL Sunday Ticket Press Copyright.
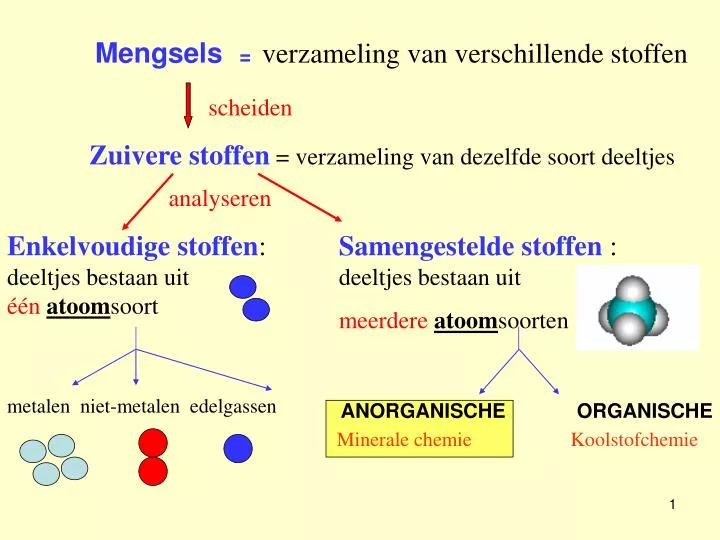
PPT Mengsels = verzameling van verschillende stoffen PowerPoint Presentation ID367110
Het verschil tussen zuivere stoffen en mengsels komt aan de orde. Ook wordt het begrip scheiden behandeld. In deze video met uitleg voor scheikunde gaan we het hebben over stoffen en mengsels. We bespreken zuivere stoffen, mengsels, vloeistoffen, legeringen, suspensies en emulsies. Zuivere stof We noemen dit zuivere stoffen en mengsels. Zuivere stoffen bestaan uit 1 stof. Ze hebben dan ook maar 1 soort molecuul. Mengsels bestaan uit 2 of meer zuivere stoffen en hebben 2 of meer soorten moleculen. Je kunt de moleculen zelf natuurlijk niet zien. Zelfs met een microscoop kun je de moleculen niet zien. In de video hiernaast kun je zien. Zuivere stoffen: Uitzicht: overal dezelfde kleur EN Bij testen: dezelfde stofeigenschappen Mengsels: Uitzicht: duidelijk verschillende stoffen OF Bij testen: verschillende stofeigenschappen Zijn er nog oefeningen op het herkennen van een zuivere stof en een mengsel?

PPT 7. Scheiden van zuivere stoffen en mengsels PowerPoint Presentation ID469841
In ijs hebben de water moleculen wel een vaste plaats en kun je ze met je hand niet verplaatsen. Op deze pagina vind je een video en uitleg over zuivere stoffen en mengsels. Daarnaast staat er onderaan een quiz om te checken of je het snapt! Wat is het verschil tussen een ZUIVERE STOF en een MENGSEL? 1.1. Een ZUIVERE STOF 1.2. Een MENGSEL 1.3. Een ZUIVERE STOF versus een MENGSEL - PROEF 1 1.4. Een ZUIVERE STOF versus een MENGSEL - PROEF 2 1.5. Een ZUIVERE STOF versus een MENGSEL - VIDEO 1.6. SAMENGEVAT 1.7. TEST JEZELF 2. Soorten MENGSELS 2.1. Een OPLOSSING - PROEF 3 2.2.
Oplossing: Suspensie: Emulsie: Tot aan de bouwstenen gemengd Helder en doorzichtig Vloeistof + vloeistof of vaste stof + vloeistof Lost niet goed op (korreltjes) Troebel en ondoorzichtig Vaste stof + vloeistof Ontmengt snel en zitten als lagen boven elkaar Troebel en ondoorzichtig Vloeistof + vloeistof Termen: Deze video hoort bij Nova 1-2 t/h, hoofdstuk 2 Stoffen, paragraaf 2 Zuivere stof en mengsels. In dit filmpje worden de begrippen moleculen, zuiver, mengsel, oplossing, suspensie, extraheren.

H1 Zuivere stoffen en mengsels Scheikunde Chemie Overal 4 VWO YouTube
2.2 zuivere stoffen en mengsels. Leerdoelen: 2.2.1 Je kunt het verschil aangeven tussen zuivere stoffen en mengsels. 2.2.2 Je kunt oplossingen en suspensies onderscheiden. 2.2.3 Je kunt beschrijven hoe je stoffen kunt scheiden door middel van extraheren of filtreren. Zuivere stoffen Indeling; Analyse; Synthese; Onderscheid mengsel en zuivere stof; Opbouw zuivere stof molecuulmodel-deeltjesmodel; begrip model; molecuulmodel. mengsels; aggregatietoestand; fysische en chemische reacties; kristalvorming; diffusie; atoommodel




